Estudios recientes han demostrado que las avispas sociales de los géneros Polistes y Vespula actúan como reservorio para la conservación de levaduras y como vectores capaces de transferir dichas levaduras a las uvas. En el siguiente trabajo, un equipo de investigadores de la Universidad de Florencia (Italia) analizó cuáles son las especies de levaduras asociadas con estas avispas y aislaron algunas cepas para su uso como agentes de bioprotección en la vinificación.
Estudio «Las avispas sociales como reservorio de levaduras no Saccharomyces para estrategias de bioprotección en la elaboración del vino» – Autores: Damiano Barbato, Simona Guerrini, Viola Galli, Eleonora Mari, Marzia Cristiana Rosi y Lisa Granchi de la Universidad de Florencia (Italia).
Estudios recientes sobre las asociaciones entre levaduras e insectos han demostrado que las avispas sociales de los géneros Polistes y Vespula actúan como reservorio para la conservación de levaduras y como vectores capaces de transferir dichas levaduras a las uvas. Este trabajo tuvo como objetivo evaluar las especies de levaduras asociadas con las avispas sociales y obtener nuevas cepas para ser utilizadas como agentes de bioprotección en la elaboración del vino.
Se determinaron las comunidades de levaduras vínicas presentes en el exoesqueleto y en el intestino de las avispas sociales, así como en la superficie de las uvas recolectadas en los viñedos de tres bodegas de la Toscana. Independientemente de la especie de avispa, las levaduras se asociaron principalmente con las obreras hembras y se encontraron sobre todo en su intestino (hasta 7 × 10⁵ UFC/mL).
La identificación reveló 20 especies pertenecientes a 10 géneros; Aureobasidium pullulans y Metschnikowia pulcherrima fueron aisladas de avispas de todas las bodegas, siendo esta última la que apareció con mayor frecuencia. La caracterización a nivel de cepa destacó que tres cepas presentes en las uvas también estaban presentes en el intestino de las avispas del mismo viñedo.
Todas las cepas aisladas de M. pulcherrima fueron sometidas a pruebas in vitro para seleccionar las más adecuadas para su uso como cultivos de bioprotección. Tres cepas mostraron una buena actividad inhibitoria contra Kloeckera apiculata y Brettanomyces bruxellensis; por lo tanto, fueron seleccionadas para ensayos de bioprotección en uvas contaminadas artificialmente.
Los resultados destacaron la reducción de poblaciones de levaduras no Saccharomyces, lo que sugiere la eficacia de M. pulcherrima como agente de biocontrol. El estudio confirmó el papel de las avispas sociales como vectores de levaduras en el viñedo y como reservorio de cepas de levaduras que pueden explotarse para aplicaciones biotecnológicas en enología.
Introducción
Las levaduras no-Saccharomyces son endémicas de los ambientes de viñedo, incluyendo el suelo y las superficies de las vides y de las uvas, y, en el momento de la cosecha, generalmente pertenecen a distintos géneros como Candida, Metschnikowia, Hanseniaspora, Cryptococcus y Rhodotorula (Barata et al., 2012). Sin embargo, la comunidad de levaduras puede cambiar con el tiempo, dependiendo de varios factores, entre ellos el estado de maduración de la uva, la ubicación del viñedo, el cultivar y las prácticas vitícolas (Griggs et al., 2021).
Además, los insectos pueden dispersar levaduras, y se ha identificado a abejas melíferas, avispas sociales y moscas del género Drosophila como vectores (Goddard et al., 2010; Lam y Howell, 2015; Stefanini et al., 2012). Los estudios sobre la dispersión de levaduras mediada por insectos sugieren que su actividad es fundamental para modelar el ensamblaje estacional del microbioma de las plantas (Madden et al., 2017, 2018).
Las levaduras colonizan principalmente el tracto digestivo de los insectos, donde pueden actuar como proveedoras de nutrientes, facilitadoras de la digestión o protectoras contra patógenos y compuestos tóxicos, resultando cruciales para el desarrollo y la supervivencia de los insectos (Malassigné et al., 2021; Stefanini, 2018).
Las avispas sociales son particularmente prometedoras como vectores potenciales de levaduras. De hecho, las reinas de Vespa crabro L. y Polistes dominulus, que hibernan como adultas, pueden transportar células de levadura desde el otoño hasta la primavera y transmitirlas a su descendencia, contribuyendo así a la supervivencia de las levaduras durante la estación desfavorable (Stefanini et al., 2012). Además, Di Paola et al. (2023) destacaron la posibilidad de utilizar P. dominulus como herramienta biotecnológica para dispersar directamente levaduras (por ejemplo, cepas de Saccharomyces cerevisiae) en el viñedo con el fin de controlar las características sensoriales del producto final.
Pocos estudios han evaluado la comunidad de levaduras transportada por estos insectos, y existe poca información sobre sus concentraciones. Stefanini y colaboradores (2012) analizaron los intestinos de 61 himenópteros (V. crabro, Polistes spp. y Apis mellifera) recolectados en Italia, encontrando que Candida fue el género más representado (43% de los aislamientos), seguido de Pichia spp. (32% de los aislamientos). La frecuencia de varias especies varió según la estación, mientras que S. cerevisiae, que constituía el 4% de la comunidad intestinal de levaduras, mostró mínimos cambios estacionales.
Otro trabajo de Jiménez et al. (2017) investigó el intestino de avispas de cinco especies en el noroeste del Pacífico. Las levaduras de los géneros Lachancea y Hanseniaspora representaron 35% de los aislamientos, 25% fueron identificados como Metschnikowia spp., y el 10% restante pertenecía a Rhodotorula. A diferencia de Stefanini et al. (2012), no se detectó S. cerevisiae en ninguna especie de avispa.
Valentini et al. (2022) demostraron que el hábitat circundante, como áreas boscosas, puede influir en las poblaciones de levaduras transportadas por las avispas hacia los viñedos. Sin embargo, algunas especies de levaduras, como Lachancea thermotolerans y Metschnikowia pulcherrima, pueden encontrarse de manera constante en el intestino de las avispas independientemente del ambiente.
Actualmente, en enología, el interés por recuperar nuevas cepas de levaduras no-Saccharomyces está aumentando debido a su potencial para mejorar el aroma del vino (Borren y Tian, 2021) y a su actividad bioprotectora (Comitini et al., 2023; Di Gianvito et al., 2022), como alternativa al uso de sulfitos para proteger los mostos, principalmente frente a posibles alteraciones causadas por la microbiota indígena en las etapas pre-fermentativas (Di Canito et al., 2021).
Entre las levaduras no-Saccharomyces, Metschnikowia pulcherrima se destaca como una de las especies más prometedoras tanto como agente de bioprotección como para mejorar el aroma del vino (Morata et al., 2019; Puyo et al., 2023). De hecho, actualmente existen cultivos comerciales de M. pulcherrima para la bioprotección de la uva, como Primaflora VB (AEB, San Polo, Italia), LEVEL2 GUARDIA™ (Lallemand, Montreal, Canadá) y ZYMAFLORE® KHIO (Laffort, Floirac, Francia).
La actividad bioprotectora puede atribuirse a varios mecanismos, como revisa Sipiczki (2020). Un papel principal lo desempeña la inmovilización del hierro mediante la producción de pulcherrimina; sin embargo, aunque la depleción de hierro es un mecanismo inhibitorio robusto, otros mecanismos también pueden contribuir a la actividad antagonista de las células de Metschnikowia, como la competencia por fuentes de nitrógeno y la secreción de quitinasas (Puyo et al., 2023).
En el presente trabajo, con el objetivo de ampliar el conocimiento sobre las especies de levaduras asociadas a las avispas sociales y obtener nuevas cepas para su uso como agentes de bioprotección en la elaboración del vino, se capturaron avispas en los viñedos de tres bodegas diferentes de la región de Toscana durante la vendimia. Las poblaciones de levaduras presentes tanto en el exoesqueleto como en el intestino fueron cuantificadas e identificadas.
Las levaduras aisladas de las avispas se compararon con las levaduras presentes en las uvas de los mismos viñedos donde se capturaron las avispas. Posteriormente, los aislamientos de M. pulcherrima fueron evaluados por su potencial de bioprotección, y los más eficaces se utilizaron para analizar su impacto en uvas contaminadas intencionalmente con especies indeseables de levaduras del vino (Hanseniaspora uvarum, Brettanomyces bruxellensis y Starmerella bacillaris) en un ensayo de bioprotección en laboratorio.
Materiales y métodos
Muestreo de insectos y uvas
Los insectos y las uvas se recolectaron en la etapa de madurez tecnológica de la uva, inmediatamente antes de la cosecha, en tres bodegas de la región de Toscana (Italia central), cada una con estatus de denominación de origen controlada y garantizada (DOCG): Chianti Classico, Brunello di Montalcino y Vino Nobile di Montepulciano.
Las bodegas se identificaron de la siguiente manera:
- MP (Villa Montepaldi—San Casciano in Val di Pesa, Florencia)
- AR (Argiano srl Società Agricola—Montalcino, Siena)
- AV (Avignonesi srl—Montepulciano, Siena)
Los viñedos fueron seleccionados en función de características similares (viñedo de Sangiovese conducido en cordón con poda de pulgar, con al menos uno de sus lados cubierto por árboles y arbustos espontáneos).
Las avispas se recolectaron durante dos días consecutivos utilizando una red entomológica y desplazándose a lo largo de las hileras del viñedo, cubriendo toda el área examinada (las superficies de los viñedos fueron de 1,2; 4,4 y 7,6 ha para las bodegas MP, AR y AV, respectivamente). Las recolecciones se realizaron durante las horas más cálidas del día, cuando las avispas estaban más activas (aproximadamente entre 10:00 y 15:00).
Posteriormente, los insectos se colocaron en tubos estériles de 50 mL y se mantuvieron refrigerados hasta su traslado al laboratorio. Una vez en el laboratorio, se introdujo en cada tubo algodón impregnado con agua esterilizada en autoclave (121 °C durante 20 min) para proporcionar una fuente de agua, evitando así la deshidratación y favoreciendo la supervivencia de las avispas. Las muestras se almacenaron a 4 °C hasta la disección, la cual se realizó dentro de las 24 horas posteriores a la recolección.
Simultáneamente al muestreo de insectos, se recolectaron uvas mediante la selección aleatoria de distintos racimos en bolsas plásticas estériles (aproximadamente 2 kg de uvas en total por viñedo), las cuales se mantuvieron refrigeradas hasta su traslado al laboratorio.
Cuantificación de levaduras en insectos y uvas
Los insectos fueron eutanasiados según el procedimiento descrito por Valentini et al. (2022), con ligeras modificaciones, mediante exposición a −21 °C durante 15 minutos. Posteriormente se procesaron para recolectar microorganismos presentes en el exoesqueleto y en el intestino.
Para determinar los microorganismos presentes en el exoesqueleto, cada insecto se colocó en tubos Eppendorf de 1,5 mL, completamente cubiertos con 300 μL de solución salina estéril (9 g/L de NaCl en agua destilada) y se sometió a sonicación durante 2 minutos (ARGOLAB DU-06, Sinergica Soluzioni S.r.l., Milán, Italia) para favorecer el desprendimiento de los microorganismos.
La solución obtenida se sembró en agar nutritivo WL (Oxoid Ltd., Basingstoke, Hampshire, Reino Unido) suplementado con: propionato de sodio (2 g/L) para inhibir el crecimiento de mohos, y estreptomicina (30 mg/L) para inhibir bacterias.
Posteriormente, las avispas fueron esterilizadas externamente mediante inmersión tres veces consecutivas en etanol al 70%, según lo descrito por Jiménez et al. (2017). El exceso de etanol se eliminó con papel absorbente estéril, y las muestras se enjuagaron con agua estéril.
Bajo condiciones estériles y utilizando un estereomicroscopio, las avispas fueron diseccionadas en placas de Petri estériles con pinzas. Se extrajo todo el tracto digestivo, incluyendo: buche o crop (intestino anterior), intestino medio e intestino posterior. Este se trituró mecánicamente con un pistilo de vidrio y se suspendió en 130 μL de solución salina estéril, aplicándose posteriormente el método de vertido en placa (pour plate).
En el caso de las uvas, se tomaron 10 g de muestra y se transfirieron a 90 mL de solución salina fisiológica estéril (9 g/L de NaCl). Las muestras se homogeneizaron durante 2 minutos en un Stomacher Lab Blender 400 (Seward Ltd., Worthing, Reino Unido).
Posteriormente, 100 μL de estas suspensiones se sembraron directamente (1 mL) o tras diluciones decimales en agar MYPG, compuesto por: 5 g/L de extracto de malta, 3 g/L de extracto de levadura, 5 g/L de extracto de carne, 10 g/L de glucosa y 20 g/L de agar. La siembra se realizó mediante el método de vertido en placa bajo condiciones estériles. Las placas se prepararon por duplicado y se incubaron durante 48 horas a 30 °C en condiciones aeróbicas. El límite de detección fue de 10 UFC/mL.
Tras la purificación, las levaduras se cultivaron en medio YEPD (10 g/L de extracto de levadura, 20 g/L de peptona y 20 g/L de dextrosa) y se conservaron a −80 °C en una solución que contenía 50% (v/v) de glicerol hasta su identificación.
Identificación y tipificación de levaduras
Tras la purificación de las colonias, las levaduras se cultivaron en medio YEPD. Los aislados fueron identificados mediante la amplificación del rDNA 5.8S y de los dos espaciadores internos transcritos ribosomales (ITS) utilizando los cebadores ITS1 e ITS4, tal como se describe en Granchi et al. (1999).
Los amplicones obtenidos se digirieron utilizando HaeIII, CfoI, HinfI y DraI como enzimas de restricción (Life Technologies Italia, Monza, Italia). Las células de levadura recogidas de colonias de 24 horas de crecimiento se suspendieron en 50 µL de agua estéril, y posteriormente 2 µL se utilizaron directamente en todas las reacciones de PCR.
Para confirmar la identificación, se amplificó el dominio D1/D2 del gen rDNA 26S, y los productos de PCR se purificaron utilizando Nucleo Spin Extract II (Macherey–Nagel GmbH & Co. KG, Düren, Alemania) siguiendo las instrucciones del fabricante antes de enviarlos a BMR Genomics (Padua, Italia) para su secuenciación. Las secuencias obtenidas en formato FASTA se compararon con las secuencias disponibles en la base de datos GenBank (http://www.ncbi.nlm.nih.gov/) utilizando las herramientas de búsqueda BLAST.
Los aislados de M. pulcherrima se tipificaron mediante análisis de ADN polimórfico amplificado al azar (RAPD) utilizando el cebador M13 (5′-GAGGGTGGCGGTTCT-3′) (Huey y Hall, 1989), según lo informado por Barbosa et al. (2018), y siguiendo el protocolo de PCR descrito por Reguant y Bordons (2003).
odas las reacciones incluyeron controles negativos (sin ADN) y positivos, y la PCR se realizó en un termociclador Applied Biosystems® 2720 (Life Technologies, Monza, Italia). La reproducibilidad de los patrones RAPD-PCR se evaluó comparando los productos de PCR obtenidos a partir de ADN preparado a partir de dos cultivos independientes de la misma cepa.
Evaluación in vitro de la actividad antimicrobiana de cepas de M. pulcherrima
La producción intracelular y extracelular de pulcherrimina se evaluó según Sipiczki (2022) con algunas modificaciones. Los cultivos de levadura se incubaron durante 24 horas a 30 °C en medio YEPD. Posteriormente, los cultivos se sembraron por puntado (spot) en placas de agar que contenían YEPD suplementado con 0,005 g/100 mL de FeCl₃. Después de 72 horas de incubación a 25 °C, las colonias que producen pulcherrimina se vuelven rojas en este medio. Si la pulcherrimina también se produce de forma extracelular, se puede observar un halo coloreado alrededor de la colonia pigmentada.
La intensidad de la pigmentación se estimó utilizando una escala de cuatro niveles:
- − = sin producción
- + = producción débil
- ++ = producción
- +++ = producción intensa
El desarrollo del halo se evaluó de la siguiente manera:
- − = ausencia de halo
- + = halo pequeño
- ++ = halo
- +++ = halo grande
La acción inhibitoria de las cepas que mostraron mayor producción de pulcherrimina se investigó posteriormente contra algunos microorganismos potencialmente alterantes del vino, específicamente: tres cepas de Brettanomyces bruxellensis y dos cepas de Kloeckera apiculata. Estas cepas pertenecían a la colección de cultivos del Departamento de Agricultura, Alimentación, Medio Ambiente y Silvicultura de la Universidad de Florencia (Italia), según lo reportado por Oro et al. (2014).
Las levaduras se cultivaron durante 24–72 horas a 30 °C en medio YEPD. Aproximadamente 10⁵ UFC/mL de los cultivos se suspendieron de manera uniforme y se incorporaron en 20 mL de agar YEPD estéril, suplementado con 0,005 g/100 mL de FeCl₃. Tras la solidificación del medio, suspensiones de M. pulcherrima (20 µL) se depositaron sobre las placas. Las placas se incubaron a 25 °C durante 3–4 días.
Después de este período, se evaluaron visualmente: el color de los puntos de M. pulcherrima y la presencia de halos de inhibición frente a cada cepa sensible. Como control, también se ensayó el cultivo iniciador comercial de M. pulcherrima LEVEL2 GUARDIA™ (Lallemand, Montreal, Canadá).
Actividad killer y sensibilidad a toxinas de las cepas de M. pulcherrima
La actividad killer de las cepas de M. pulcherrima se evaluó siguiendo el método de Philliskirk y Young (1975), utilizando como cepa sensible de referencia Saccharomyces cerevisiae (NCYC 1006; National Collection of Yeast Cultures, Norwich, Reino Unido).
Una cepa de M. pulcherrima se consideró productora de actividad killer cuando la cepa sembrada presentaba a su alrededor una zona clara en la que no se observaba crecimiento de la cepa sensible, delimitada por una zona azul oscuro de células muertas.
La sensibilidad de las cepas de M. pulcherrima a la actividad killer se evaluó sembrando la cepa killer de referencia S. cerevisiae NCYC 738 (National Collection of Yeast Cultures, Norwich, Reino Unido) sobre placas que contenían la cepa de M. pulcherrima a evaluar, incorporada en el medio de agar a una concentración aproximada de 10⁵ UFC/mL.
La cepa de M. pulcherrima se consideró sensible si no crecía alrededor de la cepa killer de referencia S. cerevisiae NCYC 738. Las cepas neutras de M. pulcherrima no producían toxina ni eran afectadas por ella.
Actividad de biocontrol de las cepas de M. pulcherrima en uvas y mostos
Las cepas de M. pulcherrima que mostraron la mayor actividad antagonista in vitro también se evaluaron por su actividad antagonista en uvas contaminadas artificialmente con especies de levaduras indeseables del vino y en el mosto resultante tras el prensado de las uvas.
Brevemente, se adquirieron uvas blancas en un supermercado local y se lavaron por inmersión en una solución de hipoclorito de sodio al 2% durante 2 minutos. Posteriormente se enjuagaron con agua destilada y se dejaron secar a temperatura ambiente para desinfectar la superficie.
Se preparó una suspensión de cultivos mixtos de: Starmerella bacillaris (10⁵ UFC/g), Kloeckera apiculata (10⁵ UFC/g),Brettanomyces bruxellensis (10² UFC/g). Las uvas se sumergieron en esta suspensión durante 2 minutos y luego se secaron bajo flujo laminar durante 2 horas.
Siguiendo el mismo protocolo, las cepas indígenas seleccionadas de M. pulcherrima y la cepa comercial LEVEL2 GUARDIA™ (Lallemand, Montreal, Canadá) se aplicaron como cultivos axénicos (10⁷ UFC/mL) sobre las uvas contaminadas para evaluar el efecto de bioprotección. Además, se preparó un control negativo sin M. pulcherrima.
Las frutas se colocaron en cajas plásticas comerciales y se almacenaron a 18 °C durante 15 horas. Posteriormente, las uvas se prensaron para obtener mosto, el cual se sometió a criomaceración durante 7 días a 6 °C.
Cada población de levaduras se cuantificó mediante el método de vertido en placa (pour plate) después de: 15 horas, y 7 días de criomaceración a 6 °C. El ensayo se realizó por duplicado.
Análisis estadístico
Los datos experimentales de recuento de levaduras se analizaron para verificar normalidad y homogeneidad de varianza, seguidos de un ANOVA de una vía y posteriormente la prueba de Tukey o la prueba de Holm–Šídák (para múltiples grupos) utilizando el software GraphPad Prism 8 (San Diego, CA, EE. UU.). Se consideró significativo un valor de p < 0,05.
Además, los perfiles RAPD-PCR obtenidos para las diferentes cepas de M. pulcherrima se sometieron a un análisis de agrupamiento mediante el método de agrupamiento de pares no ponderado con medias aritméticas (UPGMA) utilizando el coeficiente de similitud de Dice basado en bandas y el software GelCompar 6.6 (Applied Maths, St-Martens-Latem, Bélgica).
Resultados
Cuantificación e identificación de avispas y levaduras presentes en el exoesqueleto y en el intestino de las avispas
En los tres viñedos de Sangiovese considerados, se capturaron 57 avispas. La identificación de las avispas, realizada mediante la observación de sus características morfológicas (Dvořák y Roberts, 2006; Schmid-Egger et al., 2017), reveló la presencia de tres especies:
- Polistes dominulus (15,8%)
- Polistes gallicus (31,6%)
- Vespula germanica (52,6%)
Estas especies se distribuyeron de manera diferente según la bodega (Tabla 1). En los viñedos de la bodega AR, únicamente se encontró V. germanica, mientras que en los viñedos de la bodega AV se detectaron las tres especies de avispas. El 74% del total de las avispas portaban levaduras: 59% correspondían a la especie V. germanica, 24% a P. gallicus y 17% a P. dominulus (Tabla S1). Independientemente de la especie de avispa, las levaduras se asociaron principalmente con las obreras hembras.
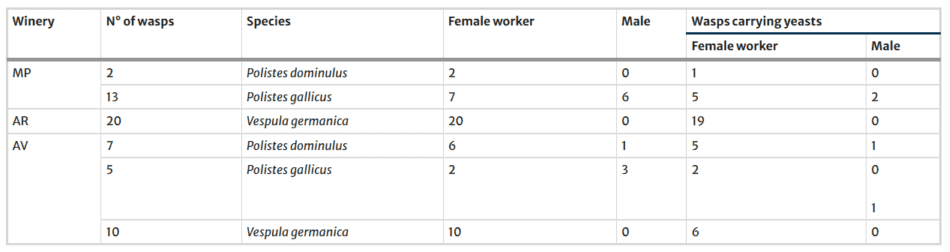
Además, se encontraron levaduras en el 67% de las avispas en el intestino, en el 19% tanto en el exoesqueleto como en el intestino, y en el 14% únicamente en el exoesqueleto (Tabla S1).
Las concentraciones de células de levadura en el intestino de las avispas, que variaron entre 7 × 10 y 7 × 10⁵ UFC/mL, fueron en promedio más altas que las cantidades de células presentes en el exoesqueleto. Sin embargo, en ambos casos no se encontraron diferencias significativas entre los datos de las tres bodegas (Fig. 1).
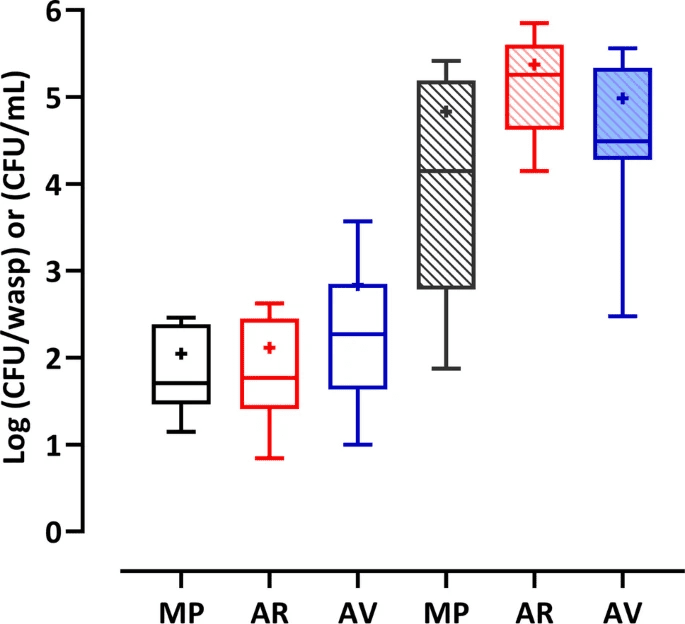
La línea central de cada caja representa la mediana, la media está indicada por el símbolo “+”, y la parte superior e inferior de la caja representan el percentil 75 y el percentil 25, respectivamente (ANOVA de una vía y prueba de Tukey, p < 0,05).
Después de cuantificar las poblaciones de levaduras asociadas con las avispas, los aislados de levaduras se identificaron mediante PCR–RFLP de la región ITS, y los resultados se presentan en la Tabla S2. La identificación reveló 20 especies diferentes de levaduras pertenecientes a 10 géneros (Aureobasidium, Candida, Cyberlindnera, Kloeckera, Lachancea, Metschnikowia, Saccharomyces, Saccharomycopsis, Torulaspora y Wickerhamomyces), incluidas en el filo Ascomycota.
En detalle, 15 especies de levaduras, incluyendo Saccharomyces cerevisiae, se asociaron con 26 avispas Vespula germanica (las cinco especies de levaduras que no se encontraron fueron A. melanogenum, C. stellata, C. agrestis, C. sake y L. thermotolerans).
Ocho especies (A. pullulans, A. melanogenum, C. stellata, M. pulcherrima, K. apiculata, C. diversa, C. agrestis y C. sake) se asociaron con nueve avispas Polistes gallicus, y cinco especies (A. pullulans, M. pulcherrima, K. apiculata, C. diversa y L. thermotolerans) con siete avispas Polistes dominulus. El 38% de las avispas que portaban levaduras albergaban una sola especie de levadura.
La distribución de las especies de levaduras según su frecuencia en las avispas capturadas en las tres bodegas, así como el número de cepas diferentes de cada especie, se muestran en la Tabla 2.
Solo el hongo levaduriforme Aureobasidium pullulans y Metschnikowia pulcherrima fueron aislados de avispas en todas las bodegas.
Además, M. pulcherrima apareció con la mayor frecuencia, independientemente de la bodega, mientras que S. cerevisiae se encontró solo en el intestino de una avispa V. germanica capturada en los viñedos de la bodega AR.
En general, S. cerevisiae estuvo escasamente presente en el intestino de las avispas, ya que solo se detectó en un único individuo.
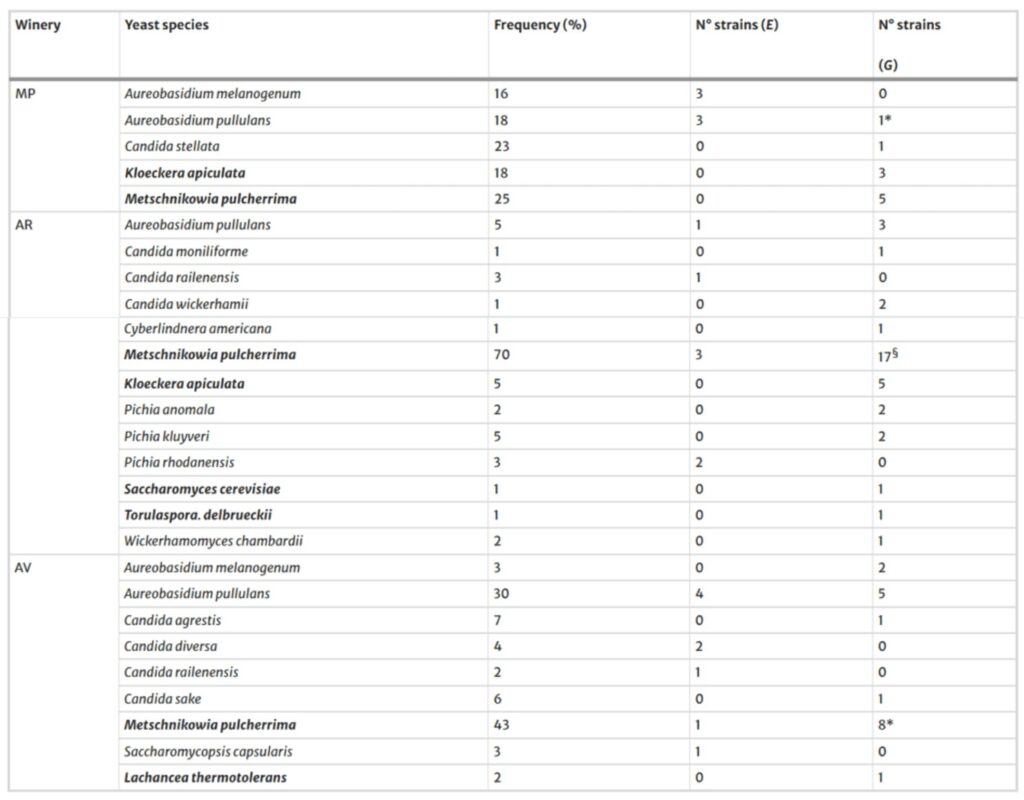
La caracterización de los aislados de levaduras a nivel de cepa reveló que 11 de las 20 especies estaban representadas cada una por una sola cepa (Tabla 2), la cual fue transportada únicamente por una avispa, ya sea en el exoesqueleto o en el intestino.
ndependientemente de la especie de levadura, las avispas provenientes de los viñedos de las tres bodegas no compartieron ninguna cepa entre sí. No obstante, en algunas avispas del mismo viñedo se encontraron cepas comunes de M. pulcherrima (datos no mostrados).
Cuantificación e identificación de levaduras presentes en uvas de Sangiovese
En los viñedos de las tres bodegas, en el momento de la cosecha y simultáneamente con la captura de avispas, se tomaron muestras de uvas Sangiovese con el objetivo de cuantificar, identificar y caracterizar a nivel de cepa las poblaciones de levaduras presentes. Las concentraciones de levaduras fueron aproximadamente de 1,5 × 10⁴ UFC/mL en las uvas de las bodegas AR y AV, y de 1 × 10⁵ UFC/mL en las uvas de la bodega MP.
Como era de esperarse, las levaduras no Saccharomyces fueron predominantes y pertenecían a Aureobasidium spp., K. apiculata y M. pulcherrima, mientras que S. cerevisiae se encontró solo en un 4% en las uvas de la bodega MP (Tabla 3).
La caracterización a nivel de cepa indicó que en las uvas de la bodega MP dos cepas (una de K. apiculata y una de M. pulcherrima) también estaban presentes en el intestino de una avispa P. gallicus capturada en el viñedo de esa misma bodega.
De manera similar, una cepa de K. apiculata encontrada en las uvas de la bodega AR también apareció en el intestino de una avispa V. germanica proveniente del mismo viñedo.
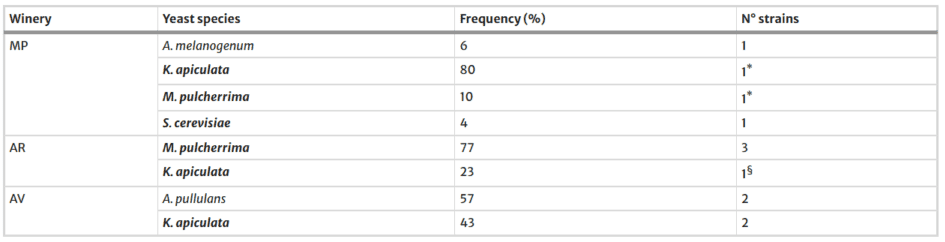
Caracterización genotípica y fenotípica de los aislados de M. pulcherrima
Metschnikowia pulcherrima fue la especie de levadura asociada con las avispas en mayor porcentaje, independientemente del viñedo de origen. Además, también fue la especie de levadura predominante en las uvas de las bodegas AR y AV.
Debido al gran interés en el uso de esta especie para la bioprotección de uvas y mostos, todos los aislados de M. pulcherrima (158) fueron caracterizados genotípicamente, encontrándose en total 30 cepas diferentes (Tabla S3).
Una o dos cepas predominantes, con una frecuencia que osciló entre el 21% y el 36%, aparecieron en la población de M. pulcherrima detectada en las avispas capturadas en los viñedos de cada bodega. Solo una cepa de M. pulcherrima también se encontró en uvas del viñedo de la bodega MP.
Para evaluar la similitud entre las cepas de M. pulcherrima, todos los diferentes perfiles RAPD-PCR (incluidos los aislados de uvas) se sometieron a un análisis de agrupamiento UPGMA utilizando el coeficiente de Dice. Con un umbral de similitud del 45%, las cepas de M. pulcherrima se agruparon en cinco clústeres distintos (Fig. 2).
- Los clústeres 1 y 5 contenían predominantemente cepas aisladas de avispas encontradas en el viñedo de una bodega (AR), lo que indica una similitud significativa relacionada con su origen de aislamiento.
- En contraste, los clústeres 2, 3 y 4 incluían cepas de M. pulcherrima derivadas de avispas recolectadas en los viñedos de las bodegas MP y AV, así como de uvas.
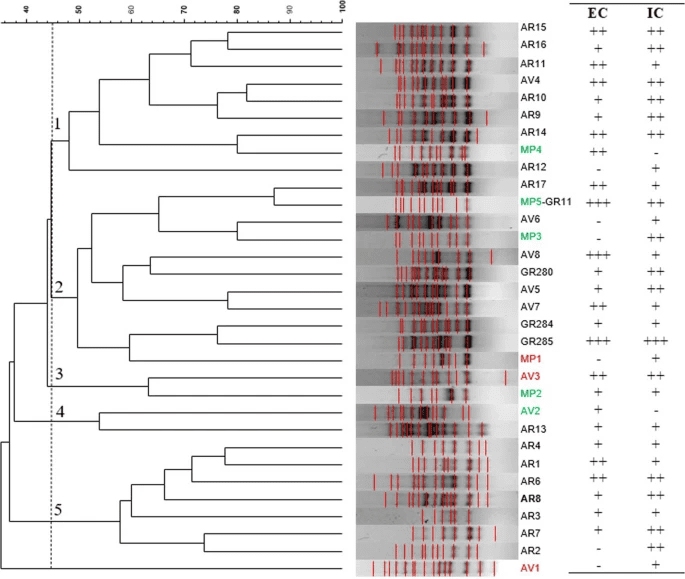
Para evaluar las propiedades bioprotectoras de las cepas de M. pulcherrima, primero se determinó su capacidad de producir el pigmento “pulcherrimina” de forma intracelular y/o extracelular, estimando respectivamente la intensidad de la pigmentación y el diámetro del halo alrededor de la colonia. Como se muestra en la Fig. 2, se observaron diferencias entre las cepas, identificándose las cepas MP5-GR11 y GR285 como las mayores productoras de pulcherrimina.
En cuanto a la actividad killer y la sensibilidad a la toxina killer, todas las cepas de M. pulcherrima analizadas resultaron neutras, es decir, no produjeron la toxina ni fueron afectadas por ella.
Actividad antimicrobiana de las cepas de M. pulcherrima: ensayo in vitro
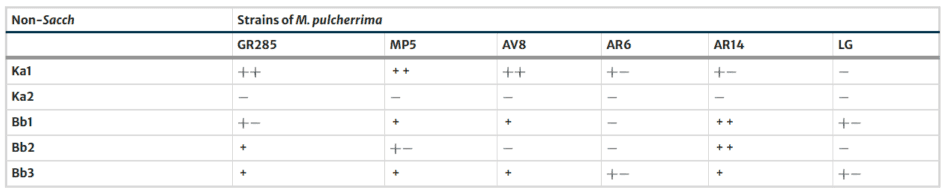
Las cepas de M. pulcherrima que mostraron mayor producción de pulcherrimina (GR285, MP5, AV8, AR6 y AR14) se evaluaron posteriormente para determinar su actividad antimicrobiana contra dos cepas de Kloeckera apiculata (Ka1 y Ka2) y tres cepas de Brettanomyces bruxellensis (Bb1, Bb2 y Bb3), dos especies de levaduras que pueden afectar negativamente la calidad final del vino.
La cepa comercial de M. pulcherrima LEVEL2 GUARDIA™ se utilizó como control. Tres de las cepas seleccionadas de M. pulcherrima (GR285, MP5 y AV8) inhibieron significativamente el crecimiento de la cepa K. apiculata Ka1; las otras dos cepas de M. pulcherrima mostraron actividad moderada, mientras que la cepa comercial no presentó efecto sobre las cepas apiculadas (Tabla 4).
En relación con B. bruxellensis, se observó sensibilidad dependiente de la cepa; únicamente la cepa M. pulcherrima AR14 fue capaz de inhibir el crecimiento de las tres cepas de B. bruxellensis evaluadas, mientras que la cepa comercial mostró una actividad débil frente a este microorganismo.
En consecuencia, las cepas silvestres derivadas de avispas demostraron mayor capacidad para inhibir levaduras de deterioro en comparación con la cepa comercial.
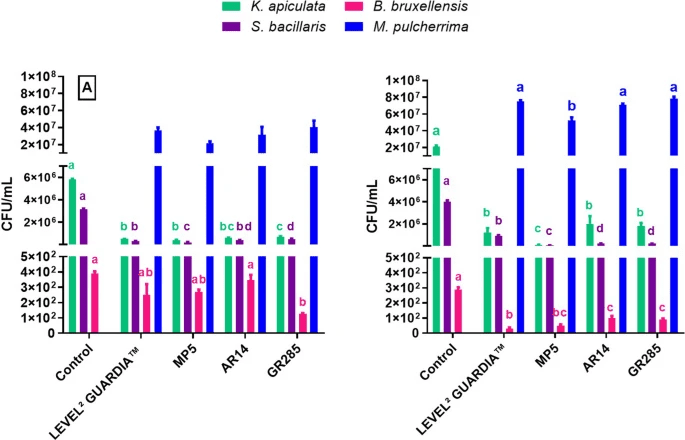
Actividad antimicrobiana de cepas de M. pulcherrima: ensayos de bioprotección
Para evaluar las capacidades reales de bioprotección de las cepas de M. pulcherrima obtenidas de avispas, las cepas seleccionadas (GR285, AR14 y MP5) se aplicaron como cultivos axénicos (10⁷ UFC/mL) sobre uvas previamente contaminadas con una mezcla de cepas de Starmerella bacillaris, Kloeckera apiculata y Brettanomyces bruxellensis.
La misma prueba se realizó utilizando la cepa comercial de M. pulcherrima LEVEL2 GUARDIA™. Posteriormente, las uvas fueron prensadas y analizadas microbiológicamente después de 15 horas a 18 °C y tras 7 días de criomaceración a 6 °C, con el objetivo de evaluar el efecto de bioprotección (Fig. 3).
Discusión
El presente estudio tuvo como objetivo evaluar a las avispas sociales como reservorio de levaduras no Saccharomyces para su uso en estrategias de bioprotección en la elaboración del vino. Con este fin, se capturaron 57 avispas durante la vendimia en viñedos de tres bodegas de la región de Toscana (Italia) y se cuantificaron e identificaron las poblaciones de levaduras presentes en su exoesqueleto y en su intestino, tanto a nivel de especie como de cepa. Paralelamente, en los mismos viñedos se recolectaron uvas maduras para la enumeración y caracterización de las levaduras presentes.
Las 57 avispas pertenecían a tres especies: P. dominulus (15,8%), P. gallicus (31,6%) y V. germanica (52,6%). Aunque el tamaño de la muestra fue pequeño, la frecuencia de individuos capturados para las diferentes especies coincide con los patrones estacionales durante la vendimia: los individuos de V. germanica son más numerosos que los del género Polistes, y las comunidades de levaduras y su abundancia son mayores en V. germanica que en las especies de Polistes (Valentini et al. 2022).
En este contexto, los resultados obtenidos respaldan el papel clave de las avispas sociales como vectores de levaduras en el ambiente, como ya se ha demostrado en otros estudios. Además, los resultados revelaron que las levaduras se encontraron con mayor frecuencia en las hembras de todas las especies, lo que sugiere una diferencia significativa entre machos y hembras en su capacidad para actuar como vectores de levaduras. Esta diferencia podría depender de sus distintos roles dentro de la colonia. Las hembras obreras realizan diversas tareas, como la búsqueda de alimento y el cuidado de las larvas, durante las cuales puede producirse la transmisión de levaduras. En contraste, los machos se centran principalmente en la reproducción y generalmente no desempeñan funciones sociales importantes.
La cuantificación de las poblaciones de levaduras asociadas a las avispas mostró que las concentraciones celulares fueron mayores en el intestino que en el exoesqueleto, independientemente de la especie de avispa y del viñedo de origen. Estos resultados confirman que el intestino de las avispas sociales alberga levaduras capaces de sobrevivir durante el invierno y reproducirse en este ambiente. Además, V. germanica hospedó más células de levadura que las especies de Polistes. Esto probablemente se deba a la capacidad de V. germanica para formar grandes colonias subterráneas, que proporcionan más fuentes microbianas.
La identificación de levaduras mostró que el hongo levaduriforme Aureobasidium pullulans y la levadura Metschnikowia pulcherrima fueron aislados de avispas capturadas en los viñedos de todas las bodegas y aparecieron con altas frecuencias. Estas especies también han sido encontradas en otros estudios en el intestino de avispas sociales.
A. pullulans también se ha detectado en los nidos de especies de Vespula, donde sus hifas parecen reforzar la estructura del nido, y además puede emitir compuestos volátiles que atraen a las avispas, lo que sugiere una posible relación mutualista. De manera similar, M. pulcherrima se encuentra comúnmente en el néctar floral, lo que indica mutualismo entre plantas y polinizadores. Además, esta levadura produce compuestos volátiles semioquímicos, como ácido acético e isobutanol, que atraen a las avispas sociales y se utilizan con frecuencia en cebos para capturarlas. Las avispas de los géneros Polistes y Vespula, que se alimentan de azúcares y flores, pueden actuar como vectores principales de esta levadura, también en los viñedos.
Entre las otras levaduras identificadas, K. apiculata, L. thermotolerans, T. delbrueckii y S. cerevisiae tienen interés enológico y aparecieron con baja frecuencia, excepto K. apiculata. A diferencia de estudios previos que indicaban la presencia de S. cerevisiae en el 4% de las avispas analizadas, en este estudio solo se encontró en el intestino de una sola avispa.
En cuanto a la cuantificación y composición de las poblaciones de levaduras en las bayas de uva en el momento de la cosecha, los resultados coinciden con los de varios estudios previos. Las comunidades de levaduras estaban compuestas principalmente por K. apiculata, A. pullulans y M. pulcherrima, mientras que S. cerevisiae se confirmó ausente o muy poco frecuente en uvas sanas.
La caracterización a nivel de cepa mostró que las avispas capturadas en cada viñedo no compartían cepas comunes entre sí. Sin embargo, se encontraron dos cepas (una de K. apiculata y una de M. pulcherrima) en el intestino de una avispa P. gallicus que también estaban presentes en las uvas del mismo viñedo. De manera similar, una cepa de K. apiculata encontrada en el intestino de una V. germanica también estaba presente en las uvas del mismo viñedo. Estos hallazgos sugieren que las avispas sociales transportan comunidades de levaduras asociadas al área local de producción, lo que respalda el concepto de terroir. Además, indican que las avispas contribuyen a la dispersión de levaduras en los viñedos al alimentarse de las uvas y romper su piel para acceder a los azúcares, lo que apoya la hipótesis de dispersión-encuentro, según la cual las levaduras son dispersadas por insectos entre recursos azucarados distantes.
En este estudio, M. pulcherrima se encontró en las avispas sociales capturadas en los tres viñedos con frecuencias de 25%, 43% y 70% de las poblaciones totales de levaduras. Debido a sus propiedades bioprotectoras bien conocidas, todas las cepas aisladas de M. pulcherrima fueron sometidas a ensayos in vitro para seleccionar las más adecuadas como cultivos bioprotectores. Tres cepas (GR285, AR14 y MP5) mostraron buena actividad inhibitoria contra K. apiculata y B. bruxellensis, dos levaduras indeseables en la vinificación. Los resultados indicaron que estas cepas no producen toxina killer, por lo que la actividad observada probablemente se deba a la formación de pulcherrimina, un quelante de hierro, que constituye el principal mecanismo de bioprotección de M. pulcherrima.
a eficacia de estas tres cepas también se demostró mediante ensayos de bioprotección a escala de laboratorio en uvas contaminadas artificialmente. Los resultados mostraron una reducción del crecimiento de levaduras no Saccharomyces tanto después de 15 horas a 18 °C como después de 7 días de criomaceración a 6 °C, lo que sugiere que M. pulcherrima podría utilizarse como agente de biocontrol en las etapas prefermentativas de la vinificación. Además, las cepas silvestres aisladas de avispas mostraron mayor capacidad bioprotectora que la cepa comercial, lo que destaca la importancia de explorar nuevas fuentes de levaduras silvestres.
Conclusiones
Este estudio confirmó el papel fundamental de las avispas sociales, especialmente las hembras obreras, como vectores de levaduras en el ambiente. Las avispas transportan cepas de levaduras presentes también en la superficie de las uvas, contribuyendo al desarrollo de comunidades microbianas características de cada región vitivinícola.
Aunque solo tres cepas de levaduras fueron comunes entre uvas y avispas, este hallazgo es relevante, ya que muy pocos estudios lo han demostrado. Las avispas sociales pueden actuar como un reservorio natural de biodiversidad, proporcionando una fuente para seleccionar cepas de levaduras con aplicaciones biotecnológicas.
En particular, cepas seleccionadas de M. pulcherrima podrían utilizarse como agentes de biocontrol, contribuyendo a reducir el uso de dióxido de azufre en la vinificación. Además, algunas cepas de esta especie presentan actividades enzimáticas que mejoran el aroma del vino, lo que la convierte en una herramienta valiosa en la enología, ya que podría mejorar el perfil aromático del vino y contrarrestar el deterioro causado por microorganismos indeseables.
Incluso se ha propuesto recientemente que alimentar a las avispas con cepas fúngicas seleccionadas de interés enológico durante periodos prolongados podría permitir modificar la microbiota fúngica del insecto según los objetivos deseados, abriendo nuevas posibilidades para aplicaciones biotecnológicas en la producción de vino.
Fuente: ACE Enología

























