Investigadores mendocinos evaluaron los efectos de dos prácticas de manejo del viñedo -enmiendas orgánicas y mallas antigranizo-sobre el microbioma del vino y los resultados de la fermentación. El estudio -publicado recientemente en la revista técnica Oeno One- se realizó durante tres vendimias consecutivas (2021 al 2023) en un viñedo de Malbec manejado de forma biodinámica y combinando métodos de cultivo microbiano, metabarcoding de bacterias y hongos, mediciones fisicoquímicas y análisis sensoriales. Los hallazgos destacaron la importancia de los hongos como bioindicadores de las prácticas de manejo del viñedo y su posible impacto en la calidad del vino.
Estudio: «Comunidades microbianas silvestres que modelan la fermentación espontánea del vino Malbec biodinámico».
Autores: Marcos Paolinelli, Laura Martínez, Santiago Sari, Aníbal Catania, Martin Uliarte, , Selva Valeria Chimeno, Sandra García Lampasona, Mariana Combina y Laura Analía Mercado del INTA EEA Mendoza; María Cecilia Lerena del Conicet; Victoria Brond y Ricardo García (por Finca Von Wigstein, Ugarteche). Publicado el 10/2/26 en la revista especializada Oeno One de la Sociedad Internacional de Viticultura y Enología (IVES).
Antes de la industrialización de la elaboración del vino, la fermentación espontánea era la única opción disponible para las bodegas, ya que dependía exclusivamente de los microorganismos nativos del viñedo debido a la ausencia de inoculantes comerciales. Aunque hoy en día la inoculación es una opción práctica para los productores a escala industrial, las pequeñas bodegas que buscan elaborar vinos distintivos pueden beneficiarse de la complejidad y singularidad de la fermentación espontánea. Sin embargo, las interacciones impredecibles entre la diversa comunidad de bacterias y hongos durante la fermentación plantean desafíos significativos. Comprender estas interacciones microbianas es esencial para tomar decisiones informadas en la elaboración del vino.
En este estudio, analizamos el microbioma, así como los perfiles fisicoquímicos y sensoriales de vinos Malbec producidos a partir de parcelas de viñedos biodinámicos sometidas a diferentes prácticas de manejo, incluyendo la incorporación de enmiendas orgánicas y la colocación de mallas antigranizo, a lo largo de tres temporadas. Nuestros resultados revelaron una heterogeneidad significativa entre fermentaciones individuales, sin efectos claros de los tratamientos del viñedo sobre los perfiles finales del vino. Notablemente, el análisis de metabarcoding mostró una notable persistencia de las firmas de ADN del consorcio fúngico nativo; específicamente, Hanseniaspora nectarophila y Hanseniaspora guilliermondii permanecieron detectables hasta el 75 % de la fermentación alcohólica (FA). Junto con Saccharomyces cerevisiae, Schizosaccharomyces japonicus y Metschnikowia pulcherrima, estas señales taxonómicas se mantuvieron constantes a lo largo de las cosechas, aunque las dos últimas fueron más sensibles a las variaciones climáticas estacionales. Estos hallazgos subrayan el papel crítico de los consorcios localmente adaptados en la configuración de la expresión única de los vinos.
Introducción
La producción moderna de vino depende en gran medida de la inoculación de levaduras, en la que se utilizan cepas comerciales para controlar el proceso de fermentación, en lugar de permitir que las levaduras indígenas presentes en el mosto inicien una fermentación espontánea (Gardner et al., 2023). La inoculación con levaduras comerciales garantiza previsibilidad, pero puede reducir la diversidad microbiana y afectar potencialmente la complejidad sensorial (Capozzi et al., 2015; Bartle et al., 2019; Philipp et al., 2021).
Los productores de vino buscan constantemente la diferenciación sensorial de sus productos, y una comprensión más profunda de las interacciones microbianas durante la fermentación podría ayudar a alcanzar sus objetivos comerciales. Sin embargo, la dinámica de las distintas poblaciones microbianas durante la fermentación espontánea, así como los cambios influenciados por la ubicación del viñedo, la sanidad de la uva y las prácticas en bodega, dificultan la predicción de su comportamiento y, en ocasiones, dan lugar a fermentaciones lentas o detenidas (Boynton & Greig, 2016).
Algunos microorganismos producen compuestos inhibitorios perjudiciales para otros, lo que resalta la necesidad de estudiar las interacciones microbianas. Esto permite mantener un equilibrio que garantice una fermentación fiable, preservando al mismo tiempo la huella microbiana del vino (Bartle et al., 2019).
En este contexto, el estudio de los recursos microbianos presentes en el viñedo es esencial para identificar el microbioma núcleo viñedo-bodega que contribuye a la producción de vinos distintivos (Stefanini & Cavallieri, 2018).
Las técnicas independientes de cultivo, como el metabarcoding, han ampliado nuestra comprensión de la diversidad microbiana más allá de los taxones tradicionales, revelando levaduras adicionales y bacterias que contribuyen a la composición del vino (Bubeck et al., 2020; Ohwofasa et al., 2024a; Ohwofasa et al., 2024b).
Un estudio reciente encontró que el 86% de los vinos en Europa contiene residuos de pesticidas debido a prácticas convencionales de manejo del viñedo destinadas a controlar enfermedades de la vid, particularmente Botrytis y la podredumbre negra (European Food Safety Authority et al., 2022).
En los últimos 20 años, el manejo orgánico de viñedos ha crecido un 600%, con las prácticas biodinámicas contribuyendo a este crecimiento, motivadas principalmente por las preferencias de los consumidores por vinos saludables, sostenibles y que expresen el terroir (da Rocha Oliveira Teixeira et al., 2023).
Las intervenciones químicas mínimas en el viñedo aseguran que solo se encuentren residuos químicos indeseables menores en el vino. Estudios recientes han demostrado que enmiendas orgánicas como el compost y el vermicompost pueden influir en la composición de la uva y del vino, proporcionando una fuente sostenible de nutrientes para los viñedos (Palenzuela et al., 2023; Rosado et al., 2022).
En Mendoza, Argentina, donde las tormentas de granizo representan un riesgo importante para la viticultura, las mallas antigranizo se utilizan ampliamente para proteger los rendimientos de uva. Más allá de su función mecánica, estas mallas modifican el microclima del viñedo —alterando la luz, la temperatura y la humedad— y pueden influir en la composición de la uva y la calidad del vino. Sin embargo, los efectos de las diferentes configuraciones de mallas antigranizo sobre las poblaciones microbianas de la uva y su impacto en las fermentaciones en los terroirs de Mendoza siguen siendo poco estudiados.
En este contexto, el objetivo de este estudio fue evaluar la influencia de dos prácticas de manejo del viñedo —enmiendas orgánicas y mallas antigranizo— durante tres vendimias consecutivas en un viñedo de Malbec manejado de forma biodinámica en Mendoza (Argentina). Combinamos métodos de cultivo microbiano, metabarcoding de bacterias y hongos, mediciones fisicoquímicas y análisis sensoriales para desentrañar los efectos relativos del manejo del viñedo y de la vendimia sobre el microbioma del vino y los resultados de la fermentación.
Materiales y métodos
1. Diseño del estudio
El estudio se llevó a cabo en un viñedo de Malbec de 1,5 ha ubicado en Ugarteche, Luján de Cuyo, Mendoza (33° 14′ 01″ S, 68° 55′ 59″ W, Figura 1A). Las vides, plantadas en 2008, han sido manejadas de forma consistente bajo un enfoque biodinámico, con aplicaciones mediante aspersión foliar de 40 g/ha de la preparación biodinámica estiércol de cuerno (500) después de la poda invernal y en la brotación; 5 g/ha de la preparación biodinámica sílice de cuerno (501) en envero, y 50 g/ha de Fladen (estiércol de vaca) después de la cosecha. El manejo fitosanitario incluyó la aplicación de aproximadamente 2 kg/ha de oxicloruro de cobre, tres veces por temporada, y 3 kg/ha de azufre elemental en la brotación. El suelo se mantuvo sin labranza, mientras que la vegetación espontánea entre las hileras del viñedo se controló mediante desmalezadoras.
El diseño experimental consistió en 18 parcelas distribuidas aleatoriamente para evaluar la aplicación de enmiendas orgánicas por triplicado: 15 toneladas/ha de vermicompost (V), 15 toneladas/ha de compost (C), y un control sin aplicación (D), combinadas con dos configuraciones de mallas antigranizo: Chapelle (CH) y Grembiule (G) (Tabla 1 y Figura 1B). En la temporada 2021, solo se evaluó el factor enmiendas (nueve parcelas) debido a un problema con la colocación de las mallas antigranizo, mientras que en 2022 y 2023 se evaluaron ambos factores. Cada parcela se designó según su combinación de tratamiento: vermicompost con Chapelle (VCH) o Grembiule (VG); compost con Chapelle (CCH) o Grembiule (CG); y control sin tratamiento con Chapelle (DCH) o Grembiule (DG).


2. Fermentaciones de mosto de uva
Se cosecharon veinte kilogramos de racimos de al menos seis plantas de vid de cada parcela evaluada y se transportaron inmediatamente al laboratorio de microbiología de la EEA Mendoza INTA. Se realizaron fermentaciones para cada parcela y, dado que las parcelas estaban replicadas por triplicado, las fermentaciones constituyen réplicas biológicas.
Los racimos se colocaron en bolsas plásticas esterilizadas, se despalillaron manualmente y se trituraron, y el mosto resultante se transfirió a un tanque plástico de 8 litros. En los mostos se determinaron pH, grados Brix, acidez total, contenido total de azúcares y densidad. La temperatura de fermentación se mantuvo entre 20–25 °C. La pérdida de peso y la densidad del mosto se monitorearon diariamente. La densidad se midió con un densímetro (Densito 30PX, Mettler Toledo Co., Columbus, OH, USA).
Tras la finalización de la fermentación alcohólica (considerada como una pérdida de peso menor a 0,5 g por día), el vino se separó del orujo y se transfirió a botellas plásticas de 2 litros, que se colocaron en una cámara con temperatura controlada (15–20 °C) para promover la fermentación maloláctica. Después de un mes, los vinos se estabilizaron en cámara fría durante dos semanas y luego se embotellaron y almacenaron durante seis meses hasta la evaluación sensorial.
La evaluación microbiológica se realizó mediante dos enfoques complementarios: (1) caracterización del microbioma mediante metabarcoding, dirigida tanto a hongos como a procariotas en una etapa avanzada de fermentación, y (2) evaluación de la población de levaduras cultivables a lo largo del proceso de fermentación.
Las muestras para cultivo microbiológico se obtuvieron al momento de colocar los mostos en los tanques (mosto fresco = M), y en tres etapas adicionales: cuando la densidad descendió a 3 g.L⁻¹ (inicio de fermentación: BF), a 30 g.L⁻¹ (mitad de fermentación: MF), a 50 g.L⁻¹ (75 % de fermentación) y a 70 g.L⁻¹, considerado el final de la fermentación alcohólica (FF). Las muestras del 75 % de fermentación de cada proceso fueron seleccionadas para el análisis de metabarcoding.
Se recolectaron 50 mL de la mezcla de fermentación en tubos plásticos estériles y se procesaron inmediatamente para obtener un pellet mediante cuatro rondas de centrifugación a 8.000 rpm a 4 °C en un equipo Thermo Scientific Sorvall ST 16R, con resuspensión en NaCl 150 mM. Los pellets lavados se almacenaron a –80 °C y se liofilizaron durante 16 horas en un liofilizador Biobase BK-FD10P. Finalmente, los pellets liofilizados se conservaron a –20 °C hasta la extracción de ADN.
3. Cultivo microbiano en placa
Para el cultivo de levaduras y hongos, se realizaron diluciones seriadas de las muestras de fermentación en agua peptonada al 0,1 % (p/v), y se sembraron en medio agar WL (Oxoid, Basingstoke, Reino Unido) con cloranfenicol (50 µg/mL) para inhibir bacterias. Tras 48 horas de incubación a 28 °C, se contaron las unidades formadoras de colonias (UFC) en placas con 10–300 colonias de cada réplica de tratamiento, sembradas por duplicado.
Las colonias se diferenciaron en levaduras Saccharomyces, levaduras no-Saccharomyces o hongos según su morfología y color. Las colonias de Saccharomyces presentaron colores crema a verde con consistencia cremosa, mientras que las levaduras no-Saccharomyces formaron colonias blancas, crema, verde grisáceo, gris azulado, rojas, crema con tonos rojizos o verde intenso con diferentes consistencias, según descripciones previas (Pallmann et al., 2001). También se identificó un grupo dentro de las levaduras no-Saccharomyces, fácilmente distinguible por la morfología de la colonia y celular, denominado levaduras apiculadas.
4. Análisis fisicoquímico
Las muestras de mosto se analizaron según métodos de la OIV (2024) para sólidos solubles (grados Brix), pH y acidez total. Las muestras de vino se analizaron con OenoFoss Wine Scan para determinar: densidad, alcohol, azúcares totales, ácido tartárico, acético, málico y láctico.
5. Análisis sensorial
La técnica sensorial utilizada fue QDA (Análisis Descriptivo Cuantitativo) para los vinos de 2021 y RATA (Rate-All-That-Apply) (Ares et al., 2014) para los vinos de 2022 y 2023. Las evaluaciones se realizaron en la sala de análisis sensorial del Centro de Estudios Enológicos (EEA Mendoza INTA). Participaron 16 panelistas.
Se realizó un análisis de varianza y un análisis de componentes principales con elipses de confianza del 95 %, utilizando los paquetes SensoMineR (Lê & Husson, 2008) y FactoMineR (Lê et al., 2008).
6. Datos climáticos
Las variables microclimáticas se monitorearon mediante una estación meteorológica AgroSens (https://ueingenieria.com/) ubicada en el viñedo. Se registraron temperaturas máximas y mínimas diarias, eventos de precipitación, velocidad del viento, radiación solar y presión atmosférica.
7. Extracción de ADN y secuenciación de amplicones
La extracción de ADN se realizó con el kit Inbio Highway DNA PuriPrep Soil, utilizando aproximadamente 100 mg del pellet de vino liofilizado. La calidad e integridad del ADN extraído se evaluaron con un espectrofotómetro DeNovix y electroforesis en gel de agarosa al 1,5 %.
El ADN extraído se envió a la plataforma Integral Microbiome Resources en Dalhousie (Canadá) para la amplificación de la región V3–V4 del gen 16S rDNA con los cebadores 341F y 805R, y los amplicones se secuenciaron en Illumina MiSeq 2 × 300 bp. La caracterización fúngica se realizó mediante la amplificación del ITS completo con los cebadores ITS1-F_KYO2 e ITS4_KYO1 y secuenciación en PacBio Sequel II con tecnología CCS.
Los datos generados fueron depositados en NCBI (PRJNA1229409).
8. Análisis bioinformático
Análisis de metabarcoding de procariotas: La caracterización del microbioma procariota se realizó utilizando archivos FASTQ con lecturas de la región V3–V4 del gen 16S, procesadas mediante la plataforma QIIME 2 versión 2023.7 (Bolyen et al., 2019). Según el resumen de calidad por base, las lecturas forward se recortaron a 280 pb y las reverse a 220 pb.
Tras la eliminación de quimeras, las variantes de secuencia de amplicones (ASVs) se asignaron mediante el plugin dada2 en QIIME 2. Para la clasificación taxonómica, se utilizó un clasificador previamente entrenado optimizado para la región V3–V4, derivado de la base de datos SILVA (Quast et al., 2013).
Luego de la primera clasificación, varios ASVs fueron asignados a cloroplastos, por lo que se incluyó un paso de filtrado para eliminar los ASVs clasificados como “mitocondria y cloroplasto”. Los ASVs filtrados se utilizaron para generar curvas de rarefacción y análisis de diversidad alfa y beta en QIIME 2.
Los análisis posteriores, así como los gráficos de perfiles filogenéticos y el Análisis de Coordenadas Principales (PCoA), se realizaron con los paquetes R animalcules y phylosmith (Smith, 2019; Zhao et al., 2021). El número de lecturas crudas secuenciadas y las retenidas después de cada paso de filtrado de calidad se muestran en la Tabla S1.
Análisis de metabarcoding fúngico: Las lecturas ITS de longitud completa obtenidas mediante secuenciación PacBio Sequel II se procesaron de acuerdo con el protocolo estándar del laboratorio Langille: https://github.com/LangilleLab/microbiome_helper/wiki/PacBio-CCS-Amplicon-SOP-v1-(qiime2).
En este flujo de trabajo, las lecturas de PacBio se formatearon para su uso en una pipeline de QIIME 2. Los archivos FASTQ contenían lecturas en ambas orientaciones, 5′-3′ y 3′-5′. Para estandarizar la orientación, se añadió la secuencia reverso-complementaria de cada lectura a su secuencia original. Posteriormente, se utilizó Cutadapt para conservar únicamente las lecturas en dirección 5′-3′, aplicando un filtro de longitud (300–900 pb) y eliminando aquellas lecturas que no comenzaban y terminaban con las secuencias de cebadores esperadas (TAGAGGAAGTAAAAGTCGTAA…GCAWAWCAAWAAGCGGAGGA).
Los archivos FASTQ resultantes se procesaron en QIIME 2 versión 2023.7 (Bolyen et al., 2019), especificando la entrada como “SingleEndFastqManifestPhred33V2”. La eliminación de quimeras y la identificación de ASVs se realizaron mediante el plugin dada2 en QIIME 2.
Para la clasificación taxonómica, la base de datos ITS se descargó de UNITE versión 9.0 (Abarenkov et al., 2022). Tras convertir las secuencias a mayúsculas, las secuencias de referencia y la taxonomía se importaron a QIIME 2 y se utilizaron para entrenar el clasificador mediante un modelo de Bayes ingenuo. El archivo resultante se empleó para asignar taxonomía a los ASVs identificados.
Los análisis de diversidad alfa y beta, así como los gráficos de abundancia taxonómica, se obtuvieron utilizando QIIME 2 y los paquetes de R animalcules y phylosmith (Bolyen et al., 2019; Smith, 2019; Zhao et al., 2021). El número de lecturas crudas secuenciadas y las retenidas tras cada paso de filtrado de calidad se muestran en la Tabla S2.
Resultados
1. Variación climática estacional
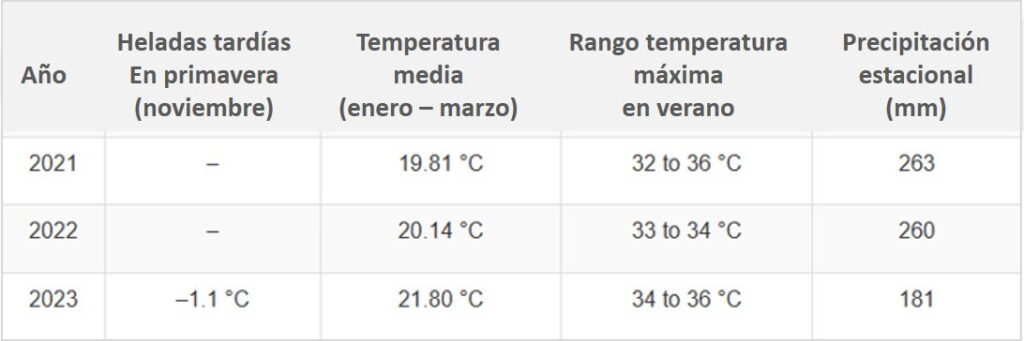
Las variables climáticas se monitorearon utilizando datos de una estación meteorológica local. Las heladas primaverales ocurrieron únicamente durante la temporada 2023. La temperatura promedio mostró una tendencia creciente, siendo 2023 el año más cálido (Tabla 2). En cuanto a las precipitaciones, las temporadas 2021 y 2022 fueron notablemente más húmedas que la temporada 2023.
2. Características del mosto y del vino
Los mostos mostraron características fisicoquímicas generales homogéneas (Tabla S3). Sin embargo, la temporada tuvo un efecto significativo sobre los sólidos solubles totales, la densidad y el pH, siendo el mosto de 2022 el que presentó los valores más bajos.
Las características microbianas generales del mosto se evaluaron mediante siembra en placa. Los recuentos de levaduras, expresados como unidades formadoras de colonias (UFC), se obtuvieron tras el cultivo en el medio diferencial y selectivo previamente descrito. En el mosto fresco, los recuentos de levaduras oscilaron entre 10⁴ y 10⁵ UFC/mL (Tabla S3).
Los recuentos de microorganismos viables se informan para cada tratamiento y reflejan la variación entre réplicas biológicas, lo cual es característico de este tipo de viñedo, conocido por su alta heterogeneidad.
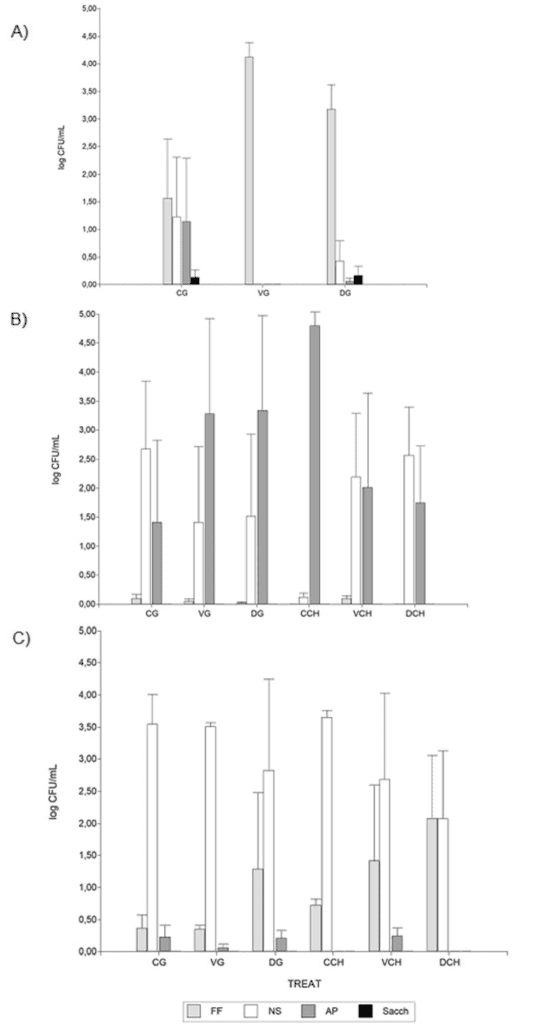
También se evidenciaron diferencias estacionales en las poblaciones microbianas. En 2021, los hongos filamentosos (FF) predominaron en las muestras de mosto. En cambio, en 2022, las levaduras apiculadas (AP) y las levaduras no-Saccharomyces (NS) se volvieron más prevalentes, mientras que los hongos estuvieron casi ausentes. En 2023, las levaduras NS fueron significativamente más abundantes y los hongos filamentosos también estuvieron presentes (Figura 2).
Las levaduras del género Saccharomyces estuvieron generalmente ausentes en los mostos, excepto en algunos casos en 2021.
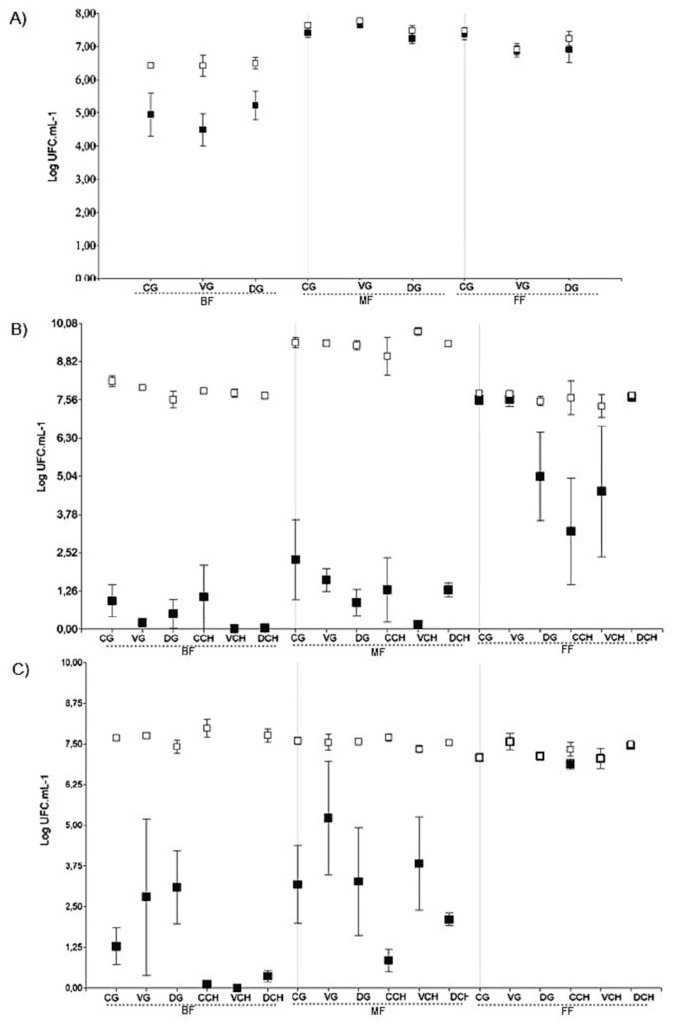
Se observaron diferencias asociadas a la vendimia en el desempeño de la fermentación, particularmente en la evolución de los recuentos de Saccharomyces —la principal levadura fermentativa— y en los recuentos totales de levaduras. En la vendimia 2021, Saccharomyces predominó en todas las etapas de la fermentación en todos los tratamientos (Figura 3A). En contraste, durante la vendimia 2022, Saccharomyces estuvo presente en proporciones muy bajas o completamente ausente al inicio de la fermentación (muestras BF). Se observó un ligero aumento en la etapa MF y, en la etapa FF, tres tratamientos mostraron dominancia de Saccharomyces, mientras que en los otros tres su proporción permaneció baja (Figura 3B).
La vendimia 2023 siguió un patrón similar al de 2022; sin embargo, se registraron mayores recuentos de UFC para Saccharomyces en la etapa MF y, en la etapa FF, este género de levaduras se volvió completamente dominante en todas las muestras (Figura 3C). Las muestras que no presentaron dominancia de Saccharomyces en la etapa FF mostraron un mayor contenido de azúcares residuales y menores niveles de etanol (tratamientos DG, CCH y VCH en la vendimia 2022; Figura 3B y Tabla S4).
3. Perfil de la comunidad procariota
Se obtuvieron un total de 1.141.157 lecturas de la región 16S-V3–V4 y, tras el recorte por calidad, la desnoisificación con dada2, el ensamblaje y la eliminación de quimeras, se retuvieron 164.659 lecturas (Tabla S1). Las curvas de rarefacción indicaron que la profundidad de secuenciación fue suficiente para capturar la mayor parte de la diversidad taxonómica (Figura S1).
La diversidad alfa de Shannon no se vio afectada por la aplicación de enmiendas ni por las configuraciones de mallas antigranizo; sin embargo, en la vendimia 2022 la diversidad fue significativamente mayor que en 2021 (prueba de Wilcoxon, p < 0,01, Figura S2). La diversidad beta bacteriana estuvo influenciada por la vendimia y no por los tratamientos (prueba PERMANOVA, p < 0,05, Figuras S2 y S4).
La comunidad procariota predominante (definida como taxones con abundancia relativa > 0,01) estuvo compuesta por 4 filos, 5 clases, 10 órdenes y 13 familias. Los géneros dominantes fueron Pantoea, Ralstonia, Gluconobacter y Tatumella, mientras que el 10,6 % de las secuencias permanecieron sin identificar (Figura 4A).
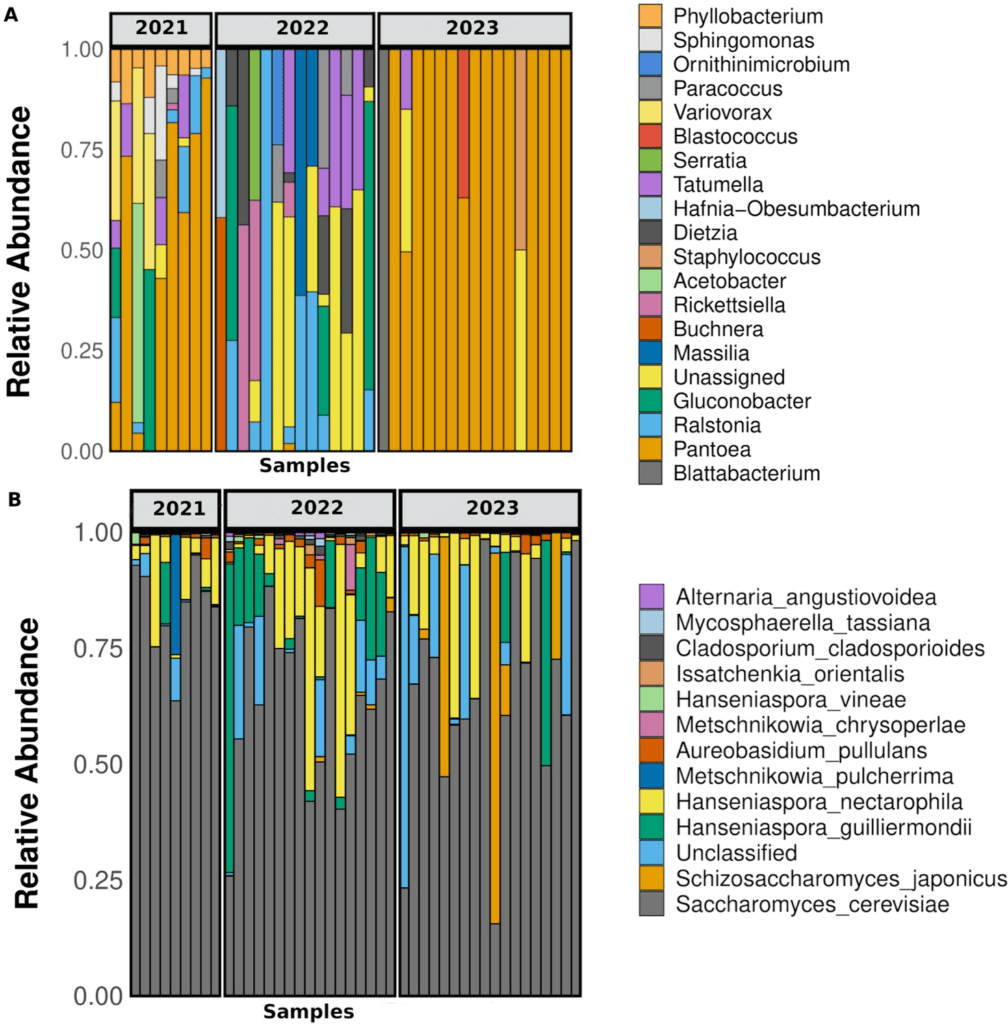
No se observaron diferencias significativas en la abundancia de taxones entre los tratamientos de campo en ninguna de las tres vendimias evaluadas (prueba DESeq2, valor p ajustado < 0,05).
Al comparar las vendimias, Pantoea fue la bacteria dominante en muchas muestras de las vendimias 2021 y 2023, pero estuvo completamente ausente en 2022 (Figura 4A). Ralstonia y Gluconobacter estuvieron presentes en algunas muestras de 2021 y 2022, pero no en 2023; Acetobacter solo estuvo presente en dos muestras de 2021, y Tatumella apareció en algunas muestras de 2022 y 2021 y solo en una de 2023 (Figura 4A).
4. Perfil de la comunidad fúngica
La secuenciación completa de ITS mediante la plataforma PacBio Sequel generó 434.271 lecturas. Tras el filtrado de calidad, se retuvieron 399.716 lecturas de alta calidad. Las curvas de rarefacción mostraron una meseta en todas las muestras (Figura S5), lo que indica una profundidad de secuenciación suficiente para capturar la diversidad.
La diversidad de Shannon no se vio afectada por los tratamientos en el viñedo, pero fue mayor en la temporada 2022 en comparación con 2021 (prueba de Wilcoxon, p < 0,01, Figura S6). La diversidad beta fúngica se modificó según la vendimia y como efecto de la configuración de las mallas antigranizo, pero no en función de las enmiendas (prueba PERMANOVA, p < 0,05, Figuras S3B y S7).
La clasificación taxonómica de los ASVs más abundantes (abundancia relativa > 0,001) identificó 12 especies. Debido a la alta precisión de la secuenciación de consenso circular (CCS) de PacBio y al uso de la región ITS completa, las especies fúngicas se identificaron con alta confianza (probabilidad de error < 1 %). La agrupación de ASVs contra la base de datos UNITE con un umbral de similitud del 99 % respaldó aún más la clasificación a nivel de especie. Sin embargo, el 7 % de los ASVs permaneció sin clasificar a nivel de especie, probablemente debido a la limitada representación de secuencias ITS fúngicas en las bases de datos de referencia, un desafío inherente a la taxonomía fúngica.
Las especies identificadas con alta abundancia (abundancia relativa > 0,001), listadas en orden descendente, fueron Saccharomyces cerevisiae, Hanseniaspora nectarophila, Hanseniaspora guilliermondii, Schizosaccharomyces japonicus, Aureobasidium pullulans y Metschnikowia pulcherrima (Figura 4B).
Dentro de cada vendimia, no se observaron diferencias significativas en la composición del microbioma fúngico del vino entre tratamientos (prueba DESeq2, valor p ajustado < 0,05).
Considerando el micobioma núcleo como las especies presentes en las tres vendimias, las levaduras S. cerevisiae, H. nectarophila y H. guilliermondii se detectaron consistentemente en todas ellas (Figura 4B). M. pulcherrima solo estuvo presente en alta abundancia relativa en una muestra de 2021, mientras que Schizosaccharomyces japonicus fue abundante en tres muestras de la vendimia 2023 (Figura 4B). Aureobasidium pullulans, aunque en bajas proporciones, también estuvo presente en las tres temporadas (Figura 4B).
5. Características del vino
La caracterización fisicoquímica de los vinos se llevó a cabo al finalizar el proceso de elaboración (Tabla S4), después de la estabilización y antes del embotellado.
6. Variables fisicoquímicas del vino
A pesar de las variaciones observadas en cada temporada durante la fermentación, la composición general del vino fue relativamente homogénea, con solo pequeñas diferencias significativas (Tabla S4). Algunos tratamientos presentaron dificultades para completar la fermentación alcohólica, lo que resultó en azúcares residuales en los vinos finales.
En este sentido, solo el tratamiento VG permitió un consumo adecuado de azúcares en todas las temporadas. Estas diferencias evidencian las distintas poblaciones de levaduras presentes en los mostos iniciales y las involucradas en cada fermentación (Figuras 1 y 2), así como el comportamiento microbiano complejo en vinos biodinámicos.
Estas diferencias microbianas no se reflejaron en el rendimiento de etanol, lo que sugiere que, a pesar del complejo consorcio microbiano involucrado, el proceso biodinámico posee su propio equilibrio, permitiendo la producción de vinos de calidad.
La fermentación maloláctica (FML) ocurrió de forma espontánea solo en los vinos de 2021, completándose 23 días después del trasiego. Esto se evidenció por el consumo casi total del ácido málico y la correspondiente formación de ácido láctico (Tabla S4).
7. Impacto sensorial de los tratamientos en el vino
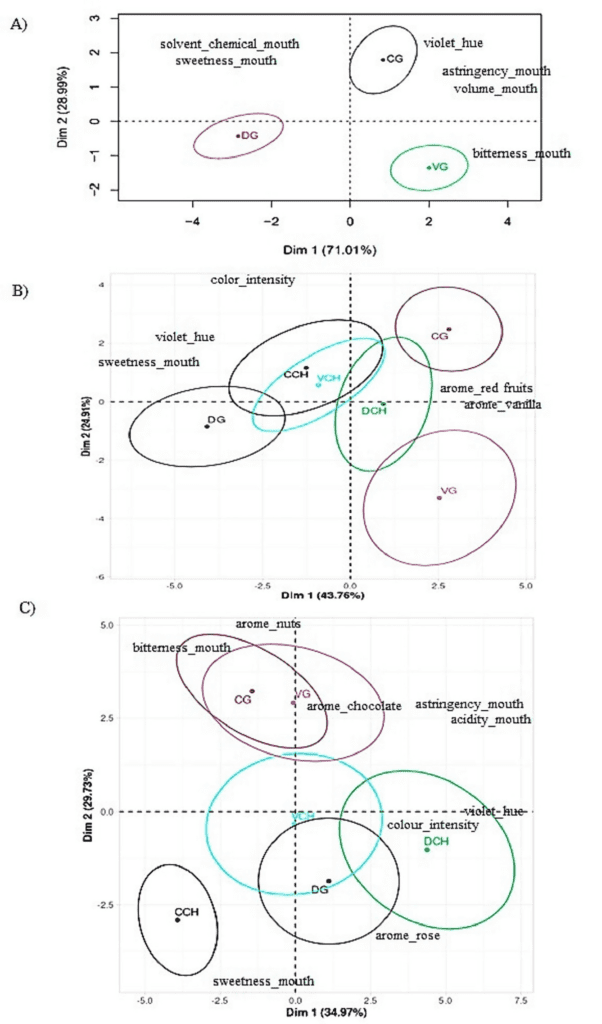
La evaluación sensorial de los vinos permitió su caracterización en función de descriptores de aroma, sensación en boca y color, revelando variaciones estacionales (Figura 5) que permitieron diferenciar los vinos.
Los vinos obtenidos en 2021 se diferenciaron en función del color (tono violáceo) y atributos básicos del gusto (dulzor, astringencia, amargor). Estos descriptores permitieron distinguir significativamente entre los tres tratamientos biodinámicos evaluados, destacándose el tratamiento VG por la diferenciación de vinos “secos”, sin azúcar residual, como se mencionó previamente.
Los vinos de la vendimia 2022 también se diferenciaron en función de atributos aromáticos distintivos, como frutas rojas y vainilla, más asociados a los tratamientos CG y VG. Nuevamente, el tratamiento VG mostró una correlación entre el consumo óptimo de azúcares durante la fermentación y una percepción de “no dulce”.
En esta temporada, fue notable la diferenciación de las características gustativas del vino encontrada por el panel entre cada tratamiento de enmienda (V, C, D) en relación con el tratamiento de malla antigranizo (G o CH), observándose una fuerte asociación del tratamiento G con descriptores aromáticos deseables.
Resultados similares se obtuvieron en los vinos de 2023, donde los vinos con tratamiento G se asociaron con el descriptor aromático de chocolate. Es interesante observar que, tras tres años de tratamiento, los vinos de CG y VG no mostraron una diferenciación clara y aparecen en la Figura 5 como elipses superpuestas.
Discusión
A diferencia de las inoculaciones controladas con cepas de levaduras seleccionadas, la fermentación espontánea depende de microorganismos presentes de forma natural, incluyendo tanto levaduras Saccharomyces como no-Saccharomyces, así como bacterias, todos los cuales pueden influir significativamente en la calidad, el aroma y la estabilidad del vino.
En el caso de fermentaciones espontáneas provenientes de viñedos manejados biodinámicamente, la caracterización del microbioma se vuelve aún más crucial, ya que estos viñedos suelen albergar una mayor diversidad microbiana que los manejados de forma convencional (Castrillo, 2022). Esta mayor diversidad genera un entorno de fermentación más complejo y competitivo, lo que resalta la importancia de comprender en profundidad las dinámicas microbianas nativas que modelan el proceso fermentativo y contribuyen a las características sensoriales únicas del vino y su expresión de terroir.
Este estudio tuvo como objetivo evaluar el impacto de diferentes prácticas de manejo del viñedo —específicamente el uso de enmiendas orgánicas y configuraciones de mallas antigranizo— sobre las comunidades de levaduras, bacterias y hongos en el vino. La estructura de la comunidad fúngica (β-diversidad) en los vinos varió según la configuración de la malla antigranizo.
En contraste, las comunidades bacterianas no se vieron afectadas. Esto sugiere que las modificaciones microclimáticas del viñedo impuestas por las mallas ejercen una presión selectiva más fuerte sobre los hongos, probablemente debido a su sensibilidad a cambios en la luz y la humedad. Por el contrario, las comunidades bacterianas parecen más resilientes, posiblemente reflejando su flexibilidad metabólica y adaptación a las condiciones del mosto. Estos hallazgos destacan la importancia de los hongos como bioindicadores de las prácticas de manejo del viñedo y su posible impacto en la calidad del vino.
La ausencia de un efecto detectable de las enmiendas sobre la α-diversidad bacteriana y fúngica en los vinos puede reflejar la alta variabilidad inherente de las vides dentro del bloque de viñedo estudiado, combinada con la influencia estabilizadora del manejo orgánico a largo plazo. Estas condiciones promueven una comunidad microbiana de base altamente diversa que podría amortiguar u ocultar los efectos específicos de los tratamientos.
Los mostos presentaron las características esperadas de uvas Malbec maduras y sanas de Mendoza (Argentina) (Fanzone et al., 2010). Los recuentos de levaduras en el mosto fresco fueron variables pero consistentes con informes previos sobre poblaciones totales de levaduras presentes en uvas Malbec maduras y sanas de Mendoza (Combina et al., 2005; Mercado et al., 2011). Asimismo, estos recuentos viables variaron según el tratamiento, la repetición y la añada, reflejando la alta heterogeneidad de este tipo de viñedo (Sun et al., 2024). Como informaron previamente Mercado et al. (2011), las levaduras Saccharomyces suelen estar ausentes en uvas frescas y mosto, un patrón confirmado por nuestros datos, salvo en algunas muestras.
Se observaron diferencias relacionadas con la añada en la dinámica de la fermentación, incluyendo la progresión de las unidades formadoras de colonias (CFU) de Saccharomyces, la principal levadura fermentativa, así como los recuentos totales de levaduras y las características resultantes del vino. Estas diferencias en las poblaciones de levaduras fermentativas asociadas al año y sus características, también conocidas como “efecto añada”, han sido reportadas previamente (Valero et al., 2007; González et al., 2020). Además, las diferencias en la finalización exitosa de la fermentación maloláctica (FML) también podrían atribuirse al efecto añada o a distintas circunstancias que afectan la progresión de la fermentación espontánea. En este sentido, es bien sabido que las levaduras pueden afectar la FML directa o indirectamente, interfiriendo con el crecimiento de bacterias malolácticas (Paramithiotis et al., 2022).
En este estudio, también se buscó comprender la relación entre las variaciones estacionales en el microbioma del vino y su influencia en la calidad. Mediante un enfoque de metabarcoding, se pudieron identificar los principales agentes microbianos que contribuyen a las fermentaciones espontáneas de vino provenientes de un viñedo en Ugarteche, Mendoza. Trabajos previos en etapas de fermentación de Malbec se realizaron en un viñedo de la provincia de Buenos Aires (Rivas et al., 2021). El presente enfoque incluye un diseño de muestreo extensivo a lo largo de tres añadas para desentrañar los agentes microbianos involucrados en la fermentación espontánea de vino Malbec en la principal región productora de esta variedad representativa de la vitivinicultura argentina.
Se observaron grandes cambios en la estructura del microbioma entre cada añada, que podrían estar relacionados con las fluctuaciones climáticas anuales, especialmente en términos de temperatura y precipitaciones (Tabla 1). Notablemente, los hongos filamentosos estuvieron ausentes en el mosto de la añada 2022, a diferencia de su presencia en 2021 y 2023 (Figura 2). Es bien conocido que los hongos filamentosos aportan un arsenal enzimático para la degradación de polímeros moleculares complejos en el mosto, liberando azúcares simples y compuestos nitrogenados asimilables que mejoran la disponibilidad de nutrientes y favorecen una fermentación alcohólica más eficiente (Viljoen, 2006). La ausencia de esta actividad enzimática podría haber contribuido al bajo rendimiento fermentativo, evidenciado por menores recuentos de S. cerevisiae en las etapas media y final de la fermentación en la añada 2022.
Además del papel fundamental y bien documentado de S. cerevisiae, también se registró la contribución de levaduras no-Saccharomyces, particularmente Hanseniaspora nectarophila y Hanseniaspora guilliermondii. Notablemente, estas especies estuvieron bien representadas en vinos de las tres añadas. Las levaduras Hanseniaspora se detectan frecuentemente en las primeras etapas de la fermentación espontánea (Albertin et al., 2016; Carrau & Henschke, 2021).
En este estudio, estas levaduras se detectaron en abundancias significativas durante el 75 % del proceso fermentativo, lo que sugiere una tolerancia moderada al etanol. La persistencia de Hanseniaspora hasta el final de la fermentación, incluso hasta 12,5 % v/v de etanol, ha sido reportada previamente (Moreira et al., 2011; Ohwofasa et al., 2024b). Varias especies del género Hanseniaspora han demostrado ser importantes como agentes enológicos, y Hanseniaspora occidentalis también ha sido reportada por reducir los niveles de ácido málico (Ohwofasa et al., 2024b). La especie H. nectarophila fue aislada por primera vez de flores de una planta nativa americana (Čadež et al., 2014) y recientemente se ha propuesto como marcador de terroir en vinos de Chipre, especialmente por su contribución a aromas florales (Kamilari et al., 2021).
Un hallazgo importante de este trabajo fue la presencia generalizada y estable de H. nectarophila, una especie no reportada previamente en estudios locales o regionales sobre levaduras de uvas y mostos. H. guilliermondii ha sido reportada por producir alcoholes superiores (como 1-propanol y 2-feniletanol), ésteres (como acetato de 2-feniletilo y acetato de etilo) y altos niveles de ácido acético (Moreira et al., 2011). Dada la persistencia de Hanseniaspora en la fermentación biodinámica estudiada y sus capacidades metabólicas, futuros estudios deberían abordar su potencial para aumentar la complejidad del vino mediante coinoculación con S. cerevisiae.
En este estudio, S. japonicus y M. pulcherrima también contribuyeron a la fermentación del vino Malbec, pero su abundancia varió significativamente entre estaciones, posiblemente debido a su mayor susceptibilidad a las fluctuaciones climáticas. Varias especies de Metschnikowia se coinoculan frecuentemente con S. cerevisiae para obtener vinos con menor contenido de etanol (Hranilovic et al., 2020). Además, M. pulcherrima se utiliza como bioprotector en mosto de uva debido a su capacidad para controlar microorganismos de deterioro (Puyo et al., 2023). Estas levaduras producen más glicerol que etanol, y este glicerol protege la membrana celular, favoreciendo la supervivencia de bacterias lácticas y promoviendo la FML (Bartle et al., 2019). Esto coincide con los resultados del estudio y podría explicar el mejor desempeño de la FML asociado a una mayor abundancia de M. pulcherrima en 2021.
Schizosaccharomyces japonicus fue particularmente abundante en la añada 2023. Esta especie es conocida por su capacidad de degradar ácido málico, reduciendo la acidez total del vino (Romani et al., 2018; Bartle et al., 2019). También promueve la liberación de polisacáridos, aumentando la viscosidad y mejorando la sensación en boca, además de contribuir a aromas frutales y florales.
La presencia de Aureobasidium pullulans —un ascomiceto dimórfico descrito como levaduriforme— en todas las fermentaciones confirma su carácter ubicuo en la microbiota de la uva y el mosto. Su prevalencia sugiere un rol ecológico clave, posiblemente facilitando la disponibilidad de azúcares fermentables y apoyando el establecimiento de S. cerevisiae.
Aunque el muestreo se realizó durante la fermentación alcohólica (FA), se plantea que las comunidades microbianas dominantes influyen en el éxito o fracaso de la FML posterior. La FML solo ocurrió en la añada 2021. Aunque se detectaron bacterias lácticas como Pediococcus, Lactococcus y Lactobacillus, su abundancia fue baja. Oenococcus oeni, la bacteria más común en FML, no fue detectada.
Las bacterias acéticas (Gluconobacter y Acetobacter) se consideran microorganismos de deterioro. Su abundancia se relacionó con condiciones húmedas, destacando la importancia del clima en la microbiota.
Pantoea fue uno de los géneros bacterianos más abundantes, aunque su rol no está claro. Tatumella también fue abundante en algunas añadas.
Este trabajo contribuye a la caracterización de la fermentación espontánea del Malbec en vinos biodinámicos, destacando un microbioma “núcleo” compuesto por S. cerevisiae, H. nectarophila, H. guilliermondii, S. japonicus y A. pullulans, además de confirmar el efecto añada en las características del vino.
Conclusión
Mediante metabarcoding, se identificaron los principales microorganismos de la fermentación espontánea del Malbec biodinámico. La variación entre añadas, influenciada por el clima, determinó la composición microbiana. Se destacaron especies de Hanseniaspora por su posible rol en las características del vino.
Es importante señalar que la presencia de microorganismos detectados no implica necesariamente actividad fermentativa. Por ello, los métodos de cultivo son esenciales para complementar estos hallazgos. Aun así, este estudio aporta información valiosa para comprender las interacciones microbianas y producir vinos que reflejen su terroir.
Este trabajo fue financiado por CAT N.º 27957/INTA–Finca Von Wigstein S.A. Se agradece a Gabriela Ruiz, Marcela González, Germán Crippa, Andrés Morales, Esteban Bolcato, Javier Barontini, Florencia Moreno y al personal del Laboratorio de Microbiología de la EEA Mendoza INTA por su colaboración durante la cosecha de uvas, el estrujado y el monitoreo del progreso de la fermentación.